Sinopharm (Пекин): BBIBP-CorV
ФАЗА 1
1 испытание
ChiCTR2000032459
Китай
ФАЗА 2
2 испытания
NCT04962906
Аргентина
ChiCTR2000032459
Китай
ЭТАП 3
6 испытаний
NCT04984408
ChiCTR2000034780
Объединенные Арабские Эмираты
NCT04612972
Перу
NCT04510207
Бахрейн, Египет, Иордания, Объединенные Арабские Эмираты
NCT04560881, BIBP2020003AR
Аргентина
NCT04917523
Объединенные Арабские Эмираты
Утверждения
Перечень использования ВОЗ в чрезвычайных ситуациях 59 Стран
Ангола, Аргентина, Бахрейн, Бангладеш, Беларусь, Белиз, Боливия (Многонациональное Государство), Бразилия, Бруней-Даруссалам, Камбоджа, Камерун, Чад, Китай, Коморские Острова, Египет, Экваториальная Гвинея, Габон, Гамбия, Грузия, Венгрия, Гай 、 Иран (Исламская Республика) 、 Ирак 、 Иордания 、 Кыргызстан 、 Лаосская Народно-Демократическая Республика
Ливан, Малайзия, Мальдивы, Мавритания, Ауритиус, Монголия, Черногория, Марокко, Мозамбик, Намибия, Непал, Нигер, Северная Македония, Пакистан, Парагвай, Перу, Филиппины, Республика Конго, Республика Конго, Энегал, Серашия, Сербия Острова 、 Сомали 、 Шри-Ланка 、 Таиланд 、 Тринидад и Тобаго 、 Тунис 、 Объединенные Арабские Эмираты 、 Венесуэла (Боливарианская Республика) 、 Вьетнам 、 Зимбабве
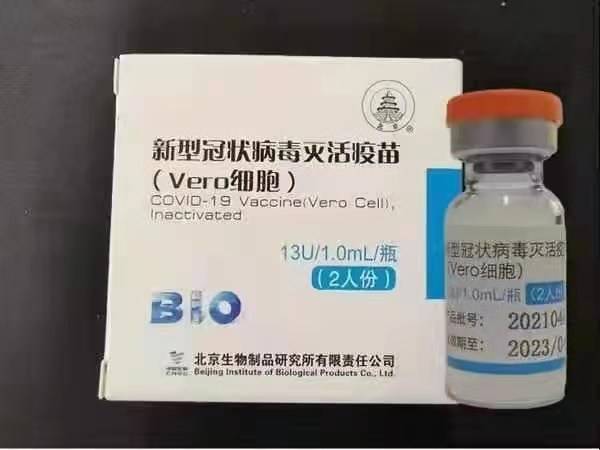
Sinopharm BBIBP-CorV COVID-19 - это инактивированная вакцина, сделанная из культивированных вирусных частиц, не обладающих патогенной способностью. Эта вакцина-кандидат была разработана Sinopharm Holdings и Пекинским институтом биологических продуктов.
Вакцина Sinopharm BBIBP-CorV работает, позволяя иммунной системе вырабатывать антитела против коронавируса SARS-CoV-2 beta. Вакцины с инактивированным вирусом, такие как вакцина против бешенства и вакцина против гепатита А, используются на протяжении десятилетий. Эта технология разработки была успешно применена ко многим хорошо известным вакцинам, таким как вакцина против бешенства.
Штамм Sinopharm SARS-CoV-2 (штамм WIV04 и номер библиотеки MN996528) был изолирован от пациента в больнице Цзиньинтань в Ухане, Китай. Вирус размножали в культуре в компетентной клеточной линии Vero, и супернатант инфицированных клеток инактивировали β-пропиолактоном (1: 4000 об. / Об., От 2 до 8 ° C) в течение 48 часов. После очистки клеточного дебриса и ультрафильтрации была проведена вторая инактивация β-пропиолактона в тех же условиях, что и первая инактивация. По данным ВОЗ, вакцина была адсорбирована на 0,5 мг квасцов и загружена в предварительно заполненные шприцы 0,5 мл стерильного физиологического раствора с фосфатным буфером без консервантов.
31 декабря 2020 года Государственное управление лекарственных средств объявило об одобрении экспериментальной вакцины, разработанной Sinopharm.
7 мая 2021 года Всемирная организация здравоохранения объявила об одобрении вакцины. Список использования ВОЗ в чрезвычайных ситуациях позволил странам ускорить получение собственных регулирующих разрешений на импорт и применение вакцины COVID-19. Консультативная группа экспертов ВОЗ по стратегиям иммунизации также завершила обзор вакцины. Основываясь на всех имеющихся данных, ВОЗ рекомендует две дозы вакцины с интервалом в три-четыре недели для взрослых в возрасте 18 лет и старше. Эффективность вакцины против симптоматических и госпитализированных заболеваний оценивается в 79% для всех возрастных групп вместе взятых.
26 мая 2021 года Американская медицинская ассоциация опубликовала «Рандомизированное клиническое испытание: влияние двух инактивированных вакцин против SARS-CoV-2 на симптоматическую инфекцию COVID-19 у взрослых», в которой говорится, что «в этом заранее определенном промежуточном анализе рандомизированного клинического исследования, взрослые. Две инактивированные вакцины против SARS-CoV-2, введенные в этом заранее определенном промежуточном анализе рандомизированных клинических испытаний, значительно снизили риск симптоматического COVID-19, а серьезные побочные эффекты были редкими ». В этом рандомизированном исследовании фазы 3 у взрослых эффективность двух инактивированных цельновирусных вакцин в симптоматических случаях COVID-19 составила 72,8% и 78,1% соответственно. Две вакцины имели редкие серьезные побочные эффекты с такой же частотой, как и в контрольной группе, получавшей только квасцы, и большинство из них не были связаны с вакцинацией. Исследовательский анализ показал, что две вакцины индуцировали измеримые нейтрализующие антитела, аналогичные результатам испытания фазы 1/2.
Рабочая группа ВОЗ SAGE опубликовала обзор вакцины Sinopharm / BBIBP COVID-19 10 мая 2021 года. Вакцина COVID-19 ГАВИ включает монитор флаконов с вакциной, который сообщает медицинским работникам, правильно ли хранилась вакцина и не подвергалась ли она воздействию перегрев. В результате, 14 мая 2021 года ГАВИ сообщил о повреждении. Смарт-этикетки, производимые Zebra Technologies и производимые Temptime Corporation, состоят из круга с более светлым квадратом посередине, сделанного из бесцветного химического вещества, которое со временем необратимо приобретает цвет. . Он становится темнее, что дает визуальное представление о совокупном тепловом воздействии. Когда флакон подвергается воздействию тепла за пределами оптимального диапазона хранения, квадрат становится темнее круга, что указывает на то, что вакцину больше не следует использовать.
Регистрационный номер национальной библиотеки лекарственных препаратов для вакцины BBIBP-CorV COVID-19: DB15807.